ETIOLOGÍA Y PATOGENIA.
Dr. Ramón García Hernández1
1- Especialista de Primer Grado en Medicina Interna. Profesor Instructor.
Jefe de Servicio de Medicina Interna
El presente trabajo va dirigido a la revisión de la etiopatogenia de esta hemoglobinopatía, que sin constituir una entidad de frecuente presentación en la práctica clínica diaria, debe tenerse presente como una de las causas de intoxicación por agentes de uso común en nuestro medio. Se actualizan los criterios del tratamiento y se proponen medidas de prevención y control.
Descriptores DeCS: METAHEMOGLOBINEMIA; CIANOSIS
El papel principal de los eritrocitos es transportar oxígeno, lo que
hacen gracias a su contenido de hemoglobina. La cantidad de oxígeno que
puede liberar en los tejidos la sangre totalmente oxigenada depende no solo
del contenido de hemoglobina y velocidad de flujo, sino de la afinidad de la
hemoglobina en el transporte del oxígeno a presiones parciales definidas.
La eficacia de la hemoglobina en el transporte de dicho elemento es entonces
resultado de su afinidad, característica particularísima que depende
de la estructura tetramétrica de la molécula de hemoglobina.1,2
La hemoglobina pura tiene una afinidad por el oxígeno demasiado alta
para que libere cantidades apreciables a las presiones parciales de oxígeno
tisular ordinarias.
Dentro del hematíe, la afinidad por el oxígeno de la hemoglobina
es modificada por varios procesos. Los iones hidrógeno estabilizan la
desoxihemoglobina y hacen menor su afinidad por el oxígeno (efecto Bohr).
El bióxido de carbono se une a la hemoglobina y disminuye su afinidad
por el oxígeno. Estas dos reacciones son las que facilitan la liberación
de oxígeno en los capilares tisulares. Ciertos fosfatos en los hematíes
reducen de forma importante la afinidad de la hemoglobina por el oxígeno;
de esta sustancias el 2-3 difosfoglicerato (DPG) se encuentra en concentraciones
mayores (casi 1 mol por mol de hemoglobina), y es la más importante en
la regulación de la disociación del oxígeno. 1-4.
La anomalías de las hemoglobinas pueden afectar el grupo hem con su átomo
de hierro, la porción globina o ambas. La oxidación del hierro
para poder formar metahemoglobina o el desplazamiento del oxígeno por
monóxido de carbono causan trastornos graves pero reversibles de la función
de la hemoglobina. Algunas sustancias tóxicas y farmacológicas,
así como bacterias pueden transformar la hemoglobina en metahemoglobina,
y pueden desnaturalizar y precipitar la hemoglobina de manera irreversible.
Las dos hemoglobinas fisiológicas, la oxihemoglobina y la hemoglobina reducida, se convierten fácilmente en una serie de compuestos por la acción de ácidos, álcalis, sustancias oxidantes y reductoras, el calor y otros agentes. Su presencia macroscópica puede distinguirse con el espectroscopio. Para pequeñas concentraciones (menos del 10%), y si se desea hacer mediciones cuantitativas, habrá que emplear métodos espectrofométricos, colorimétricos y gasométricos.
La metahemoglobina (ferrihemoglobina) es un derivado de la
hemoglobina en que el hierro ferroso se oxída a su forma férrica.
Las cadenas polipeptídicas no se alteran.
La metahemoglobina forma parte de la hemoglobina "inactiva"; es incapaz
de combinarse de modo reversible con el oxígeno y monóxido de
carbono, además desvía la curva de disociación oxígeno
en el sentido de un aumento de su afinidad por este y entorpece por tanto su
transporte desde la sangre a los tejidos. Así, cantidades anormales de
metahemoglobinemia, causarán una "anemia" funcional con cianosis
(debido a la capacidad reducida de la sangre para transportar oxígeno).
Puede haber cianosis con una concentración de 0,5 g de metaglobina por
100 cc de sangre; sin embargo el grado de cianosis no siempre estará
en proporción directa a la concentración de metahemoglobina. 4
El individuo normal puede tener hasta 0,24 g de metahemoglobina por 100 cc de
sangre: La concentración normal media es de alrededor de 0,4 % de la
hemoglobina total, o alrededor de 0,06 g/ 100 cc de sangre.
Siempre se está formando una pequeña cantidad de metahemoglobina,
pero la reducen los sistemas enzimáticos dentro del eritrocito. Según
Jaffé hay por lo menos cuatro vías por las quela metahemoglobina
puede ser reducida a hemoglobina. La más importante es el sistema de
la reductasa de la NAD - metahemoglobina. Otros que principalmente funcionan
como sistemas de reserva son el ácido ascórbico, el glutation
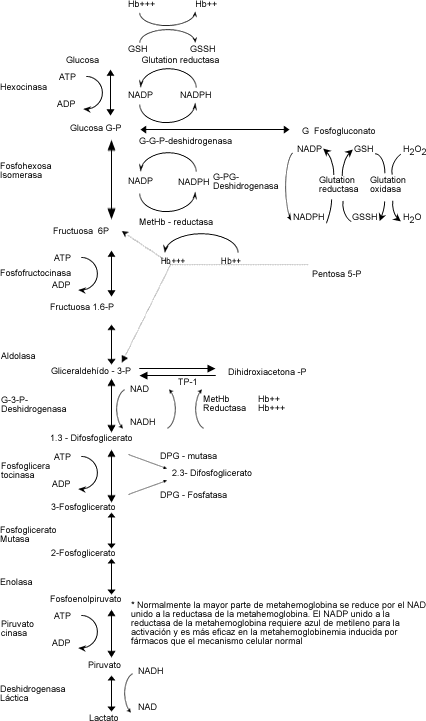
reducido, y la reductasa de NADP - metahemoglobina. (fig. 1).1
Fig.1. METABOLISMO ERITROCITARIO.

El transporte de oxígeno depende del mantenimiento intracelular
de la hemoglobina en su forma reducida (Fe 2+). Cuando la hemoglobina es oxidada
a metahemoglobina, el hierro (grupo hem) se transforma en Fe 3+ y es ahora incapaz
de fijarse al oxígeno. Normalmente las células ropas contienen
menos de 1 % de metahemoglobina como se ha dicho antes, y a ello puede contribuir
la auto-oxidación de la hemoglobina que ocurre mientras las células
circulan. Este proceso sucede por la disociación del anión superóxido
de la oxihemoglobina:
Hb2 + O2 ________________ Hb 3+ + O2-
Normalmente, la metahemoglobina formada, es reducida por la
siguiente reacción:
Hb3+ + Red Cit b5 ______________Hb2+ + OxCit b5
El Citocromo b5 reducido (RedCitb5) es generado a partir de la acción de la enzima citocromo b5 reductasa:
OxCi+b5 + NADH _______________ Red Citb5 + NAD
Desde el punto de vista patológico la metahemoglobinemia puede clasificarse
como:
Congénita: a) Déficit de citocromo b5 reductasa.
b) Alteración de las cadenas polipeptidicas de la Hb (hemoglobina M)
Adquirida: Intoxicaciones por drogas, productos químicos.
En relación a las formas congénitas, el déficit de citocromo
b5 reductasa se caracteriza por una herencia con herencia con carácter
autosómico recesivo. La enzima es una flavoproteína con propiedades
similares a la citocromo b5 reductasa microsomal hepática 5.
Los pacientes con este trastorno tienen cianosis de diversos grados de intensidad
durante toda su vida, relacionados con el nivel de metahemoglobinemia, que por
demás no se acompaña de otras manifestaciones.
Algunos pueden presentar moderada policitemia que intenta compensar las necesidades
de transportación de oxígeno tisular. En otros pacientes un ligero
retardo mental puede acompañar su evolución
Las cifras de metahemoglobina en estos pacientes pueden ser elevadas en las
postrimerías de su vida dado el envejecimiento celular y el de sus sistemas
enzimáticos ya poco competentes 5,6. En el segundo grupo de
metahemoglobinemia congénita, los sistemas reductores dentro del hematíe
son normales, pero la estructura de la molécula de hemoglobina es anormal.
Una alteración en la composición aminoacídica de dos de
las cuatro cadenas produce una molécula hemoglobínica que tiene
una tendencia aumentada a la oxidación. Se han identificado por lo menos
once hemoglobinas aberrantes asociadas a la metahemoglobinemia, que se denominan
formas diversas de la hemoglobina M ( HbM). Se heredan de forma autosómica
dominante y con excepción de la cianosis, los pacientes se mantienen
asintomáticos.
En cuanto a las metahemoglobinemias adquiridas, son las más frecuentes.
Provienen principalmente de la intoxicación por drogas y productos químicos
que causan un aumento en sangre de este tipo de hemoglobina. De manera predominante
intervienen los productos que contienen grupos nitratos o amínicos como
son la anilina y sus derivados, los nitratos, nitritos y algunas sulfamidas
entre otros1,7,8.
Los niveles de fármacos o sustancias químicas que podrían
no causar una metahemobinemia notable en un individuo normal , pueden ocasionarlas
en sujetos con leves reducción en la actividad de citocromo b5 reductasa
, quienes en circunstancias normales no estan cianóticos 1.
Se relaciona a continuación una lista de diversos factores (productos
químicos, medicamentos y bacterías) que transforman la Hb en metahemoglobina
:
Acetanilida
Acetofenetidina
Alfanaftilamina
Anilina y derivados
Paranitroanilina
Aniloetanol
Antipirina
- Bacterias-
Bacilo de Gärtner
Bacterias nitritógenas del conducto gastroentérico
Neumococo
Nitrosobacilos
Streptococo viridans
Vibrión colérico
_Benceno y derivados
Dinitrobenceno
Nitrobenceno
Nitrosobenceno
_Cloratos-
Dimetilaminas
Fenacetina
Fenilendiamina
Fenilhidroxilamina
Ferrocianuro
Formaldehído
Hidroquinona
Hidroxilacetanilida
Hidroxilamina
Metilacetanilida
Naftilamina
Nitritos
De amilo
De etilo
De sodio
Nitroglicerina
Ozono
Paraminopropriofenona
Permanganato
Peróxido de hidrogeno
Piroganol
Sulfamidas
Prontosil
Sulfanilamida
Sulfapiridina
Sulfatiazol
Sulfato ferroso
Sulfanal (sulfan-metanol)
Tolihidroxilamina
Trinitrotolueno
Yodo
La metahemoglobina vuelve a ser deducida a Hb por el sistema enzimatico de los eritrocitos. También puede reducirse lentamente mediante la administración de sustancias reductoras, tales como el ácido ascórbico o compuestos sulfihidrílicos (glutación, cisteina, BAL); estos al igual que el azul de metileno, son eficaces en un déficit hereditario de la reductasa citocromo b5 7-9.
La metahemoglobina se combina reversiblemente con varios productos químicos (por ejemplo: cianuros, sulfuros, peróxidos, fluoruros y ácidos). Por su gran afinidad por el cianuro, las intoxicaciones cianúricas deben tratarse con nitritos para formar metahemoglobina que se combina luego con el cianuro. De esta manera el cianuro libre se vuelve menos tóxico al transformarse en cianometahemoglobina.
En la metahemoglobina hereditaria la cianosis de tinte grisáceo
sucio exixte a menudo desde el nacimiento; pero este no esta asociado a dedos
hipocráticos o enfermedad cardiopulmonar. Por esto debe recordarse el
diagnóstico diferencial de la cianosis a propósito de no cometer
errores (Fig 2) 5.
El paciente con metahemoglobinemia congénita tolera concentraciones de
10 a 25 porciento sin efectos nocivos aparentes, pero de niveles superiores
a 30 % pueden asociarse con disnea leve al esfuerzo y cefalea. El retardo mental
se observa en algunos casos5.La metahemoglobinemia tóxica
si aparece rápidamente produce síntomas de anoxia. Con cifras
de 20 a 30 % aparece fatiga, disnea, taquicardia, cefalea, lipotimia, naúseas
y vómitos, aunque algunos de estos síntomas son propios del agente
causal. Con concentraciones mayores de 55 % se presentan estupor y letargo.
Por encima de 70 % de metahemoglobinemia es mortal.
Fig 2.- Diagnóstico diferencial de la cianosis.
I- Disminución de la oxigenación de la hemoglobina.
A. BAJA TENSION ARTERIAL DE OXIGENO:
1.- Enfermedad Pulmonar
2.- Shunt Cardíaco Derecha - Izquierda (comunicaciones)
B. VARIANTES DE HEMOGLOBINAS CON BAJA AFINIDAD POR O2(raro).
II- Metahemoglobinemia (raro)
A- HEREDITARIA
1- Hemoglobinas M
2- Deficiencia de citocromo b5 reductasa
III- Adquirida
1. Nitritos y nitratos: Nitrato de Sodio, Nitrato de amilo, nitroglicerina,
nitroprusiato,nitrato de plata.
2. Tintes de anilina
3. Fenacetina y acetanilina
4. Sulfonamidas
5. Otros: Lidocaína, Cloraros, fenozopiridina.
La metahemoglobinemia debe considerarse siempre entre las posibilidades
diagnósticas de todo paciente cianótico que no muestre evidencias
de enfermedad cardíaca o pulmonar. Si la cianosis es consecuencia de
una muestra de sangre de un paciente con metahemoglobinemia permanece de color
chocolate al exponerse al aire.
La metahemoglobinemia debe confirmarse con el examen espectroscópico
en el laboratorio. Los pacientes que han ingerido una droga oxidante deben tener
una hemoglobina adicional derivada llamada sulfohemoglobina en la cual la protoporfirina
ha sido químicamente modificada. La sulfohemoglobina tiende a causar
cianosis más rapidamente que la metahemoglobina. Es necesario realizar
electroforesis de Hb si se considera que las hemoglobinas M (HbM) responsable
de tal proceso 7.Son necesarios aproximadamente 5 g de desoxihemoglobina
por l00 mls de sangre para que ocurra cianosis visible; pero se aprecia un cambio
de color comparable 1,5 a 2g por ciento de metahemoglobina. La sangre que contiene
más de 10 por ciento de metahemoglobina es de color oscuro o café
y no cambia de color al mezclarse en forma intensa con el aire. Si se agregan
y mezclan unas cuantas gotas de NaCN o KCN al 10 %, rápidamente se produce
cianometahemoglobina de color rojo intenso, pero esta sustancia no afecta el
color de la sulfahemoglobina7,8.Es necesario descubrir las características
de absorción de la luz para definir la naturaleza del pigmento anormal.
La metahemoglobina ácida tiene un espectro característico con
máximas a 502 y 632 mu, que desaparecen al agregar cianuro. Las características
de absorción de la luz de las variantes de la metahemoglobina M difieren
de las de la metahemoglobina ordinaria porque sus máximos se desplazan
a longitudes de onda más baja. La velocidad de formación de un
complejo al agregar cianuro, las características del espectro de absorción
y el desplazamiento electroforético de la metahemoglobina en las variantes
de la hemoglobina normal y ayuda a establecer el diagnóstico.
El tratamiento de todo paciente intoxicado depende, además del conocimiento del agente causal, de las manifestaciones clínicas del enfermo. Teniendo en cuenta estas consideraciones a continuación se exponen los fundamentos en el manejo de las intoxicaciones; útiles para abordar cualquiera que sea la etiología y posteriormente señalaremos el tratamiento específico cuando es imprescindible realizarlo por las manifestaciones secundarias a la metahemoglobinemia 9,10.
Fundamento en el manejo de las intoxicaciones.
I- APOYO INMEDIATO
a) Protección de la vía aérea
b) Oxigenación
c) Tratar arritmias
d) Soporte Hemodinámico
e) Tratar convulsiones
f) Corregir anormalidades de temperatura.
g) Corregir anormalidades metabólicas.
h) Prevenir complicaciones secundarias.
II- PREVENCION DE FUTURAS ABSORCIONES DEL AGENTE CAUSAL.
a) Descontaminación gastrointestinal.
1-Ipecacuana
2-Lavado gástrico
3-Carbón activado
4- Enema evacuante
5-Catárticos
6-Dilución
7-Endoscopía - Remover por cirugía
b) Descontaminación de otros sitios
1- Ojos 2-Piel
III- INCREMENTAR LA ELIMINACION DEL AGENTE.
a) Dosis múltiple de carbón activado
b) Diuresis forzada
c) Altesar Ph urinario
d) Quelación
e) Métodos extracorpóreos
1- Diálisis peritoneal 5-Plasmaferesis
2-Hemodiálisis 6-Exsanguíneo transfusión
3-Hemoperfusión
4-Hemofiltración
f) Oxigenación Hiperbárica
En los casos de metahemoglobinemia tóxica las concentraciones
de 20 a 30 por ciento desaparecerán en forma espontánea en 24
a 72 horas al suspender la exposición al agente causal. Debe recurrirse
a tratamiento intensivo si ocurre inconsciencia, estupor o metahemoglobinemia
de más del 40 por ciento.
Azul de metileno. 1-2 mg 1 kg de peso corporal
Vía. Endovenosa lenta durante cinco minutos.
Puede ser necesario repetir la dosis, aunque pasados 30-60
minutos de la inyección inicial pueden ser corregidos los síntomas.
Dosis mayores de 15mg/kg han provocado hemólesis en lactantes.
En caso de no observarse mejoría evidente considérese la posibilidad
de que el paciente tenga además metahemoglobina M o sulfohemoglobina,
casos en los cuales no hay respuesta al tratamiento.
El ácido ascórbico no es recomendado pues la velocidad a la cual
este reduce la metahemoglobina es más lenta que la del proceso intrínseco
ordinario.
Por otra parte los pacientes con HbM no han respondido a formas especificas
de tratamiento , y aquellos que padecen de déficit de citocromo b5 reductasa
han mostrado una caída rápida de la metahemoglobinemia con la
administración de azul de metileno endovenosa. Además se recomienda
una dosis oral de 100 a 300 mg del medicamento para mantener por debajo del
10 porciento las concentraciones de metahemoglobina en sangre.
En los casos de metahemoglobinemia tóxica se debe insistir
por el personal médico que atiende a pacientes en riesgo sobre las medidas
estrictas destinadas a evitar el contacto. La prevención es válida
para el contacto laboral por sí mismo, como el accidental que generalmente
reúne el mayor números de casos.
Caso aparte requieren las autoridades encargadas de vigilar el uso de sustancias
nitrogenadas en el abonado de suelos, los que si alcanzan un alto grado de contaminación,
permiten que los productos agrícolas sean agentes desencadenantes de
intoxicaciones en sus consumidores. Por tanto dado el alto riesgo que esto conlleva,
cuánto se haga puede ser insuficiente a fin de evitar futuros problemas.
ALGORITMO PARA EVALUAR AL PACIENTE CIANOTICO.
Medicamento Específico
Azul de Metileno 1-2 mg x Kg x Dosis
( La dosis puede repetirse si es necesario a los 30 mts)
Nota: En una hora debe resolver el cuadro.
This work is a revision of the etiopatogenia of this hemoglobinopathy because it is frequent in our daily clinic practice. We must take in consideration that one of the main causes is the intoxication for common agents in our environment. We bring up to date the new criteria for its treatment and we propose some measures for its prevention and control.
Subjects headings: METHAHEMOGLOBINEMIA; CYANOSIS.