Indice Anterior
Siguiente
Revista de Ciencias Médicas La Habana 2000; 6 (2)
Hospital General Docente Aleida Fernández Chardiet
ACTUALIZACIÓN DEL TRATAMIENTO DE LAS HEPATITIS CRÓNICAS VIRALES.
Dr. Norlan de la Cruz Alfonso1, Dr. Rolando Martínez
López1
- Especialista de I grado en Medicina General Integral y en Gastroenterología.
RESUMEN
Las consecuencias del daño hepático por los virus
que producen lesiones crónicas constituyen un problema de salud mundial.
Se realiza una revisión actualizada del tratamiento de las Hepatitis
crónicas por virus B, C y D, con referencia a trabajos publicados en
la literatura especializada.
Descriptores DeCS: HEPATITIS CRONICA VIRAL/terapia
Los virus de la hepatitis B, D y C son los responsables de
causar hepatitis crónica, cirrosis y carcinoma hepatocelular.
Los principales países afectados por el virus B de la hepatitis son sureste
de Asia, China y Africa, que tienen una prevalencia de un 10 %. Se estima que
en los E.U.A hay 1.25 millones de personas infectadas1. Existen más
de 300 millones de portadores distribuidos por todo el mundo y mueren anualmente
2 millones de personas por la infección. En Cuba se reportan 5000 portadores
anuales, aunque después de la incorporación de la vacunación
en 1992 se redujo la enfermedad en el 50 % de los adultos, en un 96.7 % de los
niños menores de 15 años y en 92.6 % de los hijos de madres seropositivas.2,3
La prevalencia global del virus Delta es del 5% de la población mundial
(15 millones de personas infectadas) y de los casos infectados por una superinfección
más del 90% evolucionan a la cronicidad y otro grupo de estos desarrolla
una cirrosis hepática.
Por su parte, el virus C tiene una distribución mundial, se calcula que
aproximadamente 200 millones de personas están infectadas por el virus.
Es el causante del 80- 90 % de las hepatitis post-transfusionales. Se estima
que hay unos 3,5 millones de infectados en EE.UU y 700 000 en Francia. En Europa
aproximadamente 5 millones de personas están infectadas 4 . El 75- 80
% de la infección tiende a evolucionar a formas crónicas desarrollando
una cirrosis hepática en el 20 % de los casos en un curso de 10 - 20
años y de estos otro porciento ( 15- 20 %) desarrollan un carcinoma hepatocelular.5
Todos los datos anteriormente expuestos demuestran el grave problema de salud
que representa la infección crónica por los virus de las hepatitis
y la necesidad de aplicar medidas de prevención y un tratamiento eficaz
en los casos establecidos de infección crónica.
Tratamiento de la hepatitis crónica B
Los pacientes infectados con el virus de la hepatitis B ( VHB) y que tienen
el diagnóstico de hepatitis crónica requieren de tratamiento con
antivirales. El medicamento de elección es el interferón alfa
(IFN), tanto recombinante como natural, debido a su doble acción inmunomoduladora
y antiviral. Se considera que el efecto predominante del interferón en
la hepatitis B es inmunomoduladora.6
La terapéutica con interferón alfa se utiliza para lograr determinados
objetivos como seroconvertir de Ag HBe-anti HBe, que el DNA-VHB se mantenga
indetectable en el suero, lograr la seroconversión de Ag HBs-anti HBs,
suprimir de forma sostenida la replicación viral y obtener remisión
de la enfermedad hepática.
¿ Qué paciente debe ser tratado?
En la selección de los pacientes hay que tener en cuenta que el Ag HBs
se mantenga positivo por más de 6 meses de evolución para evitar
el tratamiento en los casos que seroconvierten espontáneamente en este
tiempo, deben tener positivo el Ag HBe (replicación viral estable ),
además elevación de la alaninoaminotransferasa ( ALAT) y un diagnóstico
histológico compatible con hepatitis crónica.7
Uso de interferón en la hepatitis crónica B: Regímenes
terapéuticos recomendados:
La dosis recomendada es de 10 millones de unidades (UD) de IFN, tres veces por
semana durante 4 meses7 5 millones UD diaria, subcutánea por
4 meses.8
Con este esquema de tratamiento se obtiene un 30 % de respuesta incompleta (DNA-VHB
negativo, seroconversión a anti HBe, Ag HBs positivo) y un 10 % de respuesta
completa (seroconversión de Ag HBs-anti HBs) La seroconversión
espontánea Ag HBs-anti HBs ocurre solo en un rango de 0 -10 %.7
La reactivación de la infección ocurre entre un 5 - 10 % (aproximadamente
al año de concluido el tratamiento) de los pacientes que seroconvirtieron
a anti HBe.9
Los pacientes que están infectados por el virus de la región pre-core
tienden en su mayoría a recidivar por lo que se debe utilizar pautas
más largas de tratamiento de hasta 12 meses10. Las dos mutaciones
más relevantes del VHB son: gen s, punto de mutación en posición
587, punto de mutación en posición 1896 en la región C,
asociado a un curso severo de la clínica.11
Factores predictivos asociados a respuesta favorable con el uso de interferón:7,12
- hepatitis B adquirida en la adultez.
- bajos niveles séricos de DNA-VHB
- sexo femenino.
- ALAT > 100 U/L
- intensa actividad histológica.
- paciente inmunocompetente(VIH negativo)
- escaso número de hepatocitos con tinción de los núcleos
de Ag HBc
Otros tratamientos utilizados en la Hepatitis crónica B13,14
| Terapia inmunomoduladora: |
Terapia anti-viral: |
- timosina alfa 1
- interleukina 2
- interleukina 12
- vacuna terapéutica (Ag S y pre S)
- interferón gamma
|
- lamivudina
- fanciclovir
- adefovir
- lobucavir
- ganciclovir |
Dentro del grupo de los antivirales, el más estudiado es la lamivudina.
Este anti-viral, suprime el DNA-VHB en casi todos los pacientes tratados,
del 17 al 33 % pierde el Ag HBe y el 53 al 56 % tiene una respuesta histológica
1.En un estudio americano donde se comparó el uso de lamivudina y placebo,
se encontró que el grupo tratado con el primero, seroconvirtió
(pérdida del Ag HBe y aparición de anti HBe, DNA-VHB indetectable
en el suero) en el 17 % de los casos, contra un 6 % del grupo placebo. 15
Un estudio europeo en el que se comparan 3 grupos de tratamiento, obtuvo los
siguientes resultados en cuanto a seroconversión: Un primer grupo tratado
con lamivudina (100 mg) por 8 semanas y después combinado con Interferón
10 millones de uds, 3 veces por semana durante 16 semanas hasta completar
los 6 meses (29 % seroconvirtió); el segundo grupo llevó tratamiento
coninterferón, 10 millones 3 veces por semana durante 16 semanas (16
% seroconvirtió). El tercer grupo llevó tratamiento con 100mg
de lamivudina al día durante 52 semanas (18 % de seroconversión).
Se concluye que el rango de seroconversión al año fue similar
para la monoterapia con lamivudina y el interferón durante 16 semanas.
La combinación terapéutica de lamivudina e interferón
incrementa el rango de seroconversión, particularmente en pacientes
con elevación moderada de los niveles iniciales de aminotransferasas
.16
En un año de estudio, la lamivudina fue asociada con un incremento
de la mejoría histológica en muchos pacientes con hepatitis
crónica B y una dosis diaria de 100 mg fue más efectiva que
dosis diaria de 25 mg .17
Santantonio y colaboradores18, en un seguimiento de 15 casos tratados
con 100 mg de lamivudina al día por un año, encontraron respuesta
virológica completa y ALAT normal en 11 pacientes (74 %), pero recayeron
después del tratamiento. Dos casos tuvieron respuesta virológica
y bioquímica sostenida con mejoría histológica (13 %)
y los otros dos casos recayeron a mitad de tratamiento y fueron positivos
a mutación en locus YMDD (13 %). Aquí se confirma la eficacia
de la Lamivudina para la seroconversión a anti-HBe, pero al año
de concluir la terapia la mayoría recae, observándose que la
resistencia al medicamento puede estar influenciada por mutaciones.
El transplante de hígado en la hepatitis crónica B (por cirrosis
hepática o hepatitis fulminante) se ha visto asociada a un alto rango
de reinfección. La lamivudina se ha estado utilizando para prevenir
la recurrencia viral después del transplante y la sobrevida libre de
la enfermedad es de 81 % a los 22 meses, similar a la obtenida en la terapia
con inmunoglobulinas de la hepatitis B19. En este estudio 6 pacientes
(19 %) presentaron el fenómeno de breakthrough y todos fueron positivos
con mutantes en el locus YMDD.
Mutantes del virus B resistentes a la Lamivudina 20:
La mutación YMDD confiere 10 000 veces más resistencia al tratamiento
conlamivudina.
Existen algunas diferencias entre interferón y lamivudina que se relacionan
a continuación:
LAMIVUDINA
-
Produce ligeros efectos adversos
-
No utilizar por menos de 1 año
-
Favorece mutantes resistentes
-
Seroconversión 16 - 18 % de casos INTERFERON
-
Efectos adversos importantes
-
Puede utilizarse en ciclos cortos
-
Ausencia de mutantes
-
Seroconversión 30 % de casos
Atendiendo a lo antes expuesto se debe considerar el uso
de la Lamivudina en determinados casos 21,22:
-
en pacientes que esté contraindicado el Interferón
o que no respondan al mismo.
-
para suprimir viremia antes de realizar el trasplante
hepático
-
cirrosis hepática descompensada con DNA VHB positivo
Combinaciones terapéuticas:
- interferón asociado a inmunosupresión previa con Prednisona
en pacientes con niveles basales de transaminasas < 100 U/L
- interferón asociado a Lamivudina
- lamivudina con fanciclovir
Tratamiento de la Hepatitis crónica D
Para evitar la infección por el virus D es necesario aplicar medidas
de prevención y control del virus B, pues además de tener una
forma similar de transmisión, el virus D necesita del B para multiplicarse,
de ahí la importancia del control de los donantes de sangre, la vacunación
contra el virus B de la hepatitis, evitar la promiscuidad y las enfermedades
de transmisión sexual, así como una adecuada desinfección
de instrumental, equipos, jeringuillas y agujas 23.
El interferón es el único medicamento que ha mostrado alguna eficacia
en el tratamiento de la hepatitis crónica por virus D. La mejor respuesta
se obtiene con dosis de 9 - 10 millones de unidades 3 veces por semana durante
un año, aunque la recaída es muy común al detener la terapia
24,25.
Según Carreño y colaboradores 26 alrededor del 30 % de los pacientes
tratados con Interferón, tienen una normalización de la ALAT y
pérdida del RNA-VHD, así como mejoría histológica
durante el tratamiento, pero esta respuesta no es sostenida al concluir el ciclo
y la mayoría de los pacientes recaen bioquímica y virológicamente.
La prolongación del tratamiento hasta el año parece ser mejor
en la obtención de respuesta aunque el rango de recaída es similar
cuando se compara con los cursos cortos.
Los pacientes con hepatitis crónica D coinfectados con otros virus, como
el VHC y el VIH, tienen una mala respuesta al tratamiento con el interferón.
Otros tratamientos como inmunomoduladores (levamisol), esteroides, azatioprina
y otros agentes antivirales (ribavirina) han tenido resultados negativos.
No existen hasta el momento reportes de factores relacionados con la respuesta
sostenida al tratamiento en esta infección.
Tratamiento de la Hepatitis crónica C
El screening de los anticuerpos del VHC en los donantes de sangre, fue la medida
inicial para disminuir el riesgo de transmisión del virus. En los E.U.A
esta medida ha disminuido el riesgo de infección desde un 3.84 % antes
del screening del anti-VHC a un 0.57 % después del mismo. En España,
Esteban y colaboradores, también obtuvieron una disminución del
riesgo de transmisión de la infección con la incorporación
de los anticuerpos del VHC como screening en los donantes de sangre.27
En los pacientes con hepatitis crónica C, el tratamiento con inmuno-estimulantes
y corticoides es ineficaz, solo la terapia con antivirales está justificada
en la actualidad.
Existen dos regímenes terapéuticos aprobados en la actualidad
28:
- monoterapia con interferón alfa
- terapia combinada con interferón alfa y ribavirina
La terapia combinada es más costosa y está asociada a mayores
efectos adversos que la monoterapia, pero se obtiene con ella un mayor rango
de respuesta sostenida. En estos momentos la monoterapia con Interferón
debe reservarse para pacientes que tengan contraindicaciones al uso de la ribavirina.
La dosis recomendada del interferón es de 3 millones de unidades (MU)
3 veces a la semana (3v/sem). La ribavirina se administra por vía oral
a una dosis de1000 mg para los pacientes de menos de 75 kg de peso o 1200 mg
para los de mayor peso, a dosis fraccionadas de 2 veces al día.
El National Institutes of Health (NIH) en conferencia de consenso para el manejo
de los pacientes con hepatitis crónica C, aprobó los siguientes
criterios de tratamiento29.
- Adultos de 18-60 años
- Pacientes con elevación de las aminotransferasas
- Pacientes con presencia de anti-VHC y RNA-VHC en suero
- Biopsia hepática con moderada-severa actividad necroinflamatoria,
algún grado de fibrosis y cirrosis compensada
En caso de coinfección con el virus de inmunodeficiencia, se debe realizar
conteo de CD4, ya que si la cifra es normal o mayor de 400 /ml, la respuesta
al tratamiento es similar a los pacientes no infectados por el VIH .30
Los pacientes con cirrosis descompensada, aminotransferasas normales, trasplantados
de órganos y los que tengan contraindicaciones al interferón,
no deben ser tratados 29
Figura 1 Algoritmo de tratamiento con Interferón (IFN) en la Hepatitis
crónica C.
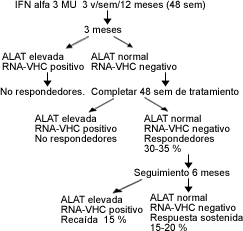
Como se observa en la Fig.1 solo el 15 al 20 % de los pacientes tratados con
IFN logran tener respuesta sostenida, lo que ha hecho que otros autores ensayen
nuevas terapias
( terapia combinada de IFN y ribavirina) en los pacientes no respondedores y
en los pacientes con respuesta completa y recaída posterior En estas
series se demuestra que la Ribavirina asociada a IFN aumenta significativamente
el índice de respuesta sostenida 31,32.
La FDA (Food and Drug Administration) aprobó en 1998 el tratamiento combinado
de IFN + ribavirina para pacientes no respondedores, recidivantes y que nunca
antes hubieran recibido tratamiento 33.
En otro estudio 34, utilizando la dosis recomendada de IFN alfa,
3 MU / 3v sem + ribavirina 1000-1200 mg al día por 6 meses, se obtuvieron
resultados similares a los descritos por Brillanti 31 y Schavarcz 32.
Como se planteó anteriormente, el tratamiento con IFN como monoterapia,
debe tener un curso de 48 semanas, aún con independencia del genotipo
viral. En el caso de los pacientes tratados con terapia combinada, la duración
óptima del tratamiento, depende del genotipo viral. Se ha visto que el
genotipo 1b tiene baja respuesta sostenida en comparación con el 2a y
335,36
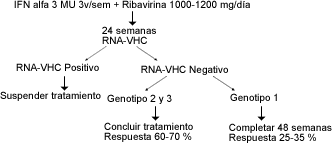
Aproximadamente el 70 % de los pacientes con genotipo 2a y 3, tienen respuesta
sostenida durante la terapia combinada y un curso de 24 semanas de duración
con esta conducta, es equivalente al curso de 48 semanas. Al contrario, los
pacientes con genotipo 1, tienen bajo porcentaje de respuesta sostenida con
terapia combinada (25-35 %) y un ciclo de 48 semanas de duración es el
recomendado (figura.2). 28
Figura 2. Algoritmo de tratamiento en la Hepatitis crónica C según
genotipo viral
¿ Qué hacer antes de la terapia ?
- Biopsia hepática para confirmar diagnóstico de hepatitis
crónica, precisar grado de actividad necroinflamatoria y estadificar
la enfermedad.
- RNA-VHC por PCR (Reacción de la Polimerasa en Cadena).
- Test de genotipo viral (ó serotipo) para manejar duración
del tratamiento.
- ALAT
- Consentimiento del paciente sobre riesgos y beneficios de la terapia.
¿Qué hacer durante la terapia ?
- Conteo hematológico: Hb, Hto, Leucocitos, Plaquetas y ALAT en
la semana 1, 2, 4 y después con intervalos de 4 - 8 semanas.
- Ajustar dosis de Ribavirina (200 mg de una vez) disminuyéndola
si Hb < 10 g/dl o Hto < 30 % y suspenderla si anemia severa (Hb <
8 g/dl o Hto < 26 %).
- RNA-VHC a las 24 semanas.
- Medir TSH (Hormona estimulante del tiroides) cada 3 meses.
- RNA-VHC al final del tratamiento para valorar respuesta.
¿Qué hacer después del tratamiento ?
-
Medir ALAT cada 2 meses por 6 meses.
-
RNA-VHC por PCR a los 6 meses de concluido el tratamiento.
Si el RNA es negativo el pronóstico es excelente (Recidivas raras)
Otros tratamientos empleados asociados al IFN.
-
Timosina alfa 1
-
Interleukina 10 y otras citokinas
-
Flebotomías
-
Antioxidantes (N - acetilcisteína)
-
AINES (Antinflamatorios no esteroideos)
-
Acido ursodesoxicólico
La timosina alfa 1 se ha empleado en la hepatitis crónica C unida
al IFN. Moscarella y colaboradores, en un estudio de 6 meses concluyeron que
esta asociación fue más efectiva que el IFN solo y que pudiera
representar una alternativa en los pacientes con esta afección.37
Se ha planteado el uso de interleukina 10 y otras citokinas como posibilidades
de asociación al IFN.38
Los pacientes no respondedores al tratamiento con IFN, tienen cifras elevadas
de hierro intrahepático y niveles elevados de ferritina, esto favorece
la oxidación en los hepatocitos con formación de radicales libres;
por lo tanto, mayor lesión y necrosis celular, de ello se deduce el
uso de flebotomías y antioxidantes en combinación con IFN.39
Se ha demostrado que el IFN produce liberación intracelular de ácido
araquidónico y su metabolito, la PG E2, tiene propiedades inmunosupresoras.
Los AINES, inhiben la vía ciclooxigenasa bloqueando la síntesis
de PG E2 y aumentan la concentración de la 2´-5´ oligoadenilato
sintetasa, enzima con acción antiviral .36
Todos estos tratamientos alternativos unidos al IFN, no han demostrado la
eficacia que se esperaba de ellos .40
Factores predictivos de respuesta al IFN en la hepatitis crónica C
.41
-
Factores que dependen del virus:
- nivel de replicación viral. RNA-VHC > 1-2 millones de copias
genómicas / ml (peor respuesta).
- genotipo viral 1b (peor respuesta)
- quasiespecies: Si tiene mayor número (peor respuesta)
-
Factores relacionados con el huésped:
- grado de actividad inflamatoria y estadio de la enfermedad
a mayor actividad, peor pronóstico
a mayor fibrosis, peor respuesta
- tiempo de infección
a mayor tiempo, peor respuesta
- enfermedades asociadas: SIDA, Insuficiencia renal crónica
peor respuesta
- sobrecarga de hierro, ferritina
peor respuesta
- colestasis
a mayor colestasis, peor pronóstico
-
Factores relacionados con el IFN:
- IFN alfa 2a, alfa 2b, menos eficaz
- leucocitario natural y linfoblastoide, más eficaz
- anticuerpos anti-IFN, peor pronóstico
El factor predictivo de remisión a largo plazo es lo que sucedió
a los 6 meses de concluido el tratamiento: respuesta bioquímica y
virológica sostenida.
Interferón pegilado
Más recientemente se está empleando una formulación de
interferón alfa de acción prolongada, el cual se realiza por unión
de los componentes del IFN alfa y el polietilenglicol que forma una larga cadena
que se conoce como IFN-PEG (interferón pegilado) y es administrado subcutáneamente
1 vez a la semana, con menos efectos adversos que el estándar y con el
cual se obtienen picos mantenidos en sangre de hasta 90 horas o más y
se habla de que tiene resultados similares a los logrados con la terapia combinada
de IFN estándar y ribavirina 33,40.
En la actualidad se están desarrollando nuevos agentes que incluyen inhibidores
de las enzimas virales como son los inhibidores de las proteasas, las helicasas
y polimerasas. La vacunación es otra alternativa y en estos momentos
se están realizando grandes esfuerzos para lograr su obtención
con vistas a desarrollar acciones preventivas.42
REFERENCIAS BIBLIOGRÁFICAS.
- Malik AH, Lee WM. Chronic hepatitis B virus infection: treatment strategies
for the next millennium. Ann Intern Med 2000; 132:723-31.
- Valdés García L. Enfermedades emergentes y reemergentes.
La Habana: Ministerio de Salud Pública; 1998.
- Delgado González G, Galindo Sardiña MA, Pérez Blanco
P. Hepatitis B en Cuba: década de los 90 y más allá
del 2000. En: Centro de Ingeniería Genética y Biotecnología.
Aplicaciones médicas de la biotecnología. Biotecnología
Habana' 99; 1999 Nov 28 - Dic 3 La Habana. La Habana: Elfos Scientiae; 1999.pp.O20-O21.
- Alter MJ. Epidemiology of hepatitis C. J Gastroenterol Hepatol 1996;
8:319-23.
- Strader DB, Seeff LB. The natural history of chronic hepatitis C infection.
J Gastroenterol Hepatol 1996; 8: 324-8.
- Padrón GJ. Bases moleculares para el estudio de las hepatitis
virales. La Habana: Elfos Scientiae; 1998.
- Scully LJ. Treatment of chronic hepatitis B virus infection. Can J Gastroenterol
1997; 11:17-20.
- Di Bisceglie AM. Long-term outcome of interferon-alpha therapy for chronic
hepatitis B. J Hepatol 1995; 22:65-7.
- Perrillo RP. Interferon therapy of chronic hepatitis B. En: Arroyo V,
Bosh J, Rodes J, Eds. Treatments in hepatology. Barcelona: Masson; 1995.pp.141-53.
- Perrillo RP. Chronic hepatitis B: problem patients (including patients
with decompensated disease). J Hepatol 1995; 22:45-8.
- Grob PJ. Hepatitis B:virus, pathogenesis and treatment. Vaccine 1998;
16:11-6.
- Minuk YG. Principles in the management of chronic hepatitis B viral infection.
(review) Can J Gastroenterol 1999; 13:75-7.
- Nicoll A, Locarnini S. Present and future directions in the treatment
of chronic hepatitis B infection. (review) J Gastroenterol Hepatol 1997;
12: 843-54.
- Morrey JD, Korba BE, Sidwell RW. Transgenic mice as a chemotherapeutic
model for hepatitis B virus infection. Antivir Ther 1998; 3:59-68.
- Dienstag JL, Schiff ER, Wright TL, Perrillo RP, Hann HWL, Goodman Z,
et al. Lamivudine as initial treatment for chronic hepatitis B in the United
States. N Engl J Med 1999; 341:1256-63.
- Schalm SW, Heathcote J, Cianciara J, Farrell G, Sherman M, Willems B,
et al. Lamivudine and alpha interferon combination treatment of patients
with chronic hepatitis B infection: a randomised trial. Gut 2000; 46:526-8.
- Lai C-L, Chien R-N, Leung NWY, Chang T-T, Guan R, Tai D-I, et al. A one-year
trial of lamivudine for chronic hepatitis B. N Engl J Med 1998; 339:61-8.
- Santantonio T, Mazzola M, Iacovazzi T, Miglietta A, Guastadisegni A,
Pastore G. Long-term follow-up of patients with anti-HB e/ HBV DNA-positive
chronic hepatitis B treated for 12 months with lamivudine. J Hepatol 2000;
32:300-6.
- Malkan G, Cattral MS, Humar A, AL Asghar H, Greig PD, Hemming AW, et
al. Lamivudine for hepatitis B in liver transplantation: a single-center
experience. Transplantation 2000; 69:1403-7.
- Rey D, Fritsch S, Schmitt C, Partisani M, Kempf-Durepaire G, Nicolle
M, et al. Emergence of resistan hepatitis B virus strains during long-term
lamivudine therapy in human inmunodeficiency virus co-infected patients.
Gastroenterol Clin Biol 2000; 24:125-7.
- Petry W, Erhardt A, Heintges T, Haussinger D. New developments in therapy
of chronic hepatitis B. When are nucleoside analogs indicated? Z Gastroenterol
2000; 38:77-87.
- Renner EL. Hepatitis B: when to use lamivudine? Schweiz Med Wochenschr
2000; 130:39-41.
- Huo T-I, Wu J-C, Lin R-Y, Sheng W-Y, Chang F-Y, Lee S-D. Decreasing hepatitis
D virus infection in Taiwan: An analysis of contributory factors. J Gastroenterol
Hepatol 1997; 12:747-51.
- Farci P, Mandas A, Coiana A, Lai ME, Desmet V, Van Eyken P, et al. Treatment
of chronic hepatitis D with interferon alpha-2 a. N Engl J Med 1994; 330:88-94.
- Van Leewen DJ, Dadrat A. Viral hepatitis and its imitators I: women's
medicine. En: Blackwell RE, Ed. Cambridge: Blackwell Science; 1996.pp.324-38.
- Carreño V, Bartolomé J, Madejón A. Hepatitis delta
virus infection: molecular biology and treatment. Dig Dis 1994; 12:265-75.
- González A, Esteban JI, Madoz P, Viladomiu L, Genesca J, Muñiz
E, et al. Efficacy of screening donors for antibodies to the hepatitis C
virus to prevent transfusion-associated hepatitis: final report of a prospective
trial. Hepatology 1995; 22:882-5.
- National Institutes of Health. Chronic Hepatitis C: current disease management.
New York: NIH; 2000 [Publication no 99-42 30].
- National Institutes of Health. Consensus development conference: management
of hepatitis C. Hepatology 1997; 26 (Suppl 1).
- Spengler U, Rockstroh JK. Hepatitis C in the patient with human inmunodeficiency
virus infection. J Hepatol 1998; 29: 1023-30.
- Brillanti S, Miglioli M, Barbara L. Combination antiviral therapy with
ribavirin and interferon alfa relapsers and non-responders: Italian experience.
J Hepatol 1995; 23:13-6.
- Schvarcz R, Ando Y, Sonnenborg A, Weiland O. Combination treatment with
interferon alfa-2b and ribavirin for chronic hepatitis C in patients who
have failed to achieve sustained response to interferon alone: swedish experience.
J Hepatol 1995; 23:8-12.
- Lam NP. Hepatitis C: natural history, diagnosis and management. Am J
Health-Syst Pharm 1999; 56:961-76.
- Mc Hutchison JG, Gordon SC, Schiff ER. Interferon alfa-2b alone or in
combination with ribavirin as initial treatment for chronic hepatitis. N
Engl J Med 1998; 339:1485-92.
- Lai MY. Firstline treatment for hepatitis C: combination interferon/ribavirin
interferon monotherapy. J Gastroenterol Hepatol 2000; 15:130-3.
- Olaso V, Córdoba J, Prieto M. Tratamiento de la hepatitis crónica
C. Rev Esp Enf Dig 1997; 89:621-37.
- Moscarella S, Buzzelli G, Romanelli RG, Monti M, Giannini C, Careccia
G, et al. Interferon and thymosin combination therapy in naive patients
with chronic hepatitis C: preliminary results. Liver 1998; 18:366-9.
- Levine RA. Treating histologically mild chronic hepatitis C: monotherapy,
combination therapy, or tincture of time? Ann Intern Med 1998; 129:323-6.
- Van Thiel DH, Friedlander L, Mallory P, Fagivoli S, Wright HI, Gasbarrin
A, et al. Re-treatment of hepatitis C interferon non-responders with larger
doses of interferon with and withaut phlebotomy. Gastroenterology 1994;
106:1002.
- Arús Soler E. Estado actual del tratamiento de las hepatitis virales
crónicas. Jornadas LUSO-Cubanas de Gastrenterologia em Medicina Geral
e Familiar; 2000 Jul 21-26; Varadero. Lisboa: Faculdade de Ciencias Médicas
de Lisboa; 2000.pp.36-39.
- Kobayashi M, Chayama K, Arase Y, Tsubota A, Saitoh S, Susuki Y, et al.
Predictive value of different hepatitis C serological assays in the treatment
of chronic hepatitis C with interferon a. J Gastroenterol 1999; 34:94-9.
- Gish GR. Future directions in the treatment of patients with chronic
hepatitis C virus infection. Can J Gastroenterol 1999; 13:57-62.
SUMMARY.
The consequence of the hepatic damage by virus with produce
chronic lesions constitute a problem of the world health. An up-to- date revision
of the treatment of the chronic B, C and D hepatitis was done with reference
of the published works in the specialized literature.
Subjet headings: HEPATITIS, CHRONIC VIRAL/theraphy
Indice Anterior
Siguiente

